
【文献速递】肿瘤类器官+芯片,提升药敏检测时效性
2021年5月10日清华大学联合北大人民医院、北京航天航空大学将微流控芯片与肿瘤类器官结合,开发出全新的集成超疏水微孔阵列芯片(InSMAR-chip),可在一周内获得肿瘤类器官药敏预测结果,显著提高了对肿瘤患者抗癌药物临床疗效预测的效率和时效,将该成果发表于学术期刊《Nature Communications》。
LCOs培养及其特性
研究者采用机械处理方法,从103例手术切除和活检肿瘤组织建立肺癌类器官(lungcancer organoids,LCOs),成功率79%,其中包括腺癌(AC)71例、鳞状细胞癌(SCC)23例、小细胞肺癌(SCLC)4例和其他类型的肺癌5例。
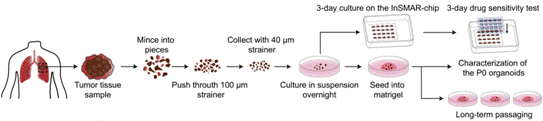
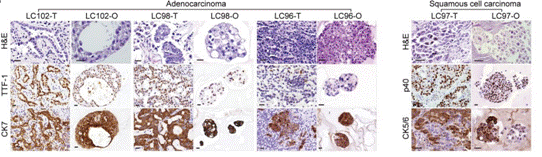
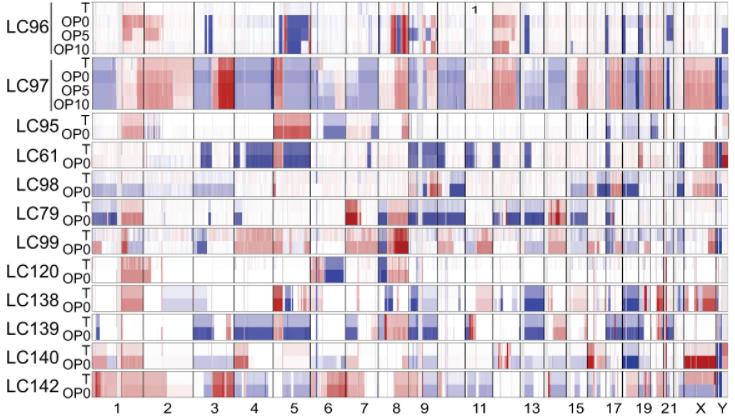
建立的LCOs保留了亲代肿瘤的组织学与遗传学特征,并具有无限传代扩增的潜力。图2HE染色结果和图3的全基因组拷贝数变异分析显示LCOs具有与体内肿瘤一致的组织结构和蛋白基因表达模式。
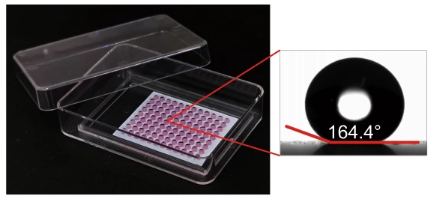
InSMAR-chip
InSMAR-chip具有通量高、体积小、节约样本和试剂并可进行实时追踪和寻址的特征,其表面由于注入了超疏水涂层,使得微孔之间具有物理隔绝,保证了每个微孔独立的液体环境,便于加样和换液的操作,此外,芯片微孔间距与1536孔板保持一致,更适配商用的成像及检测仪器。
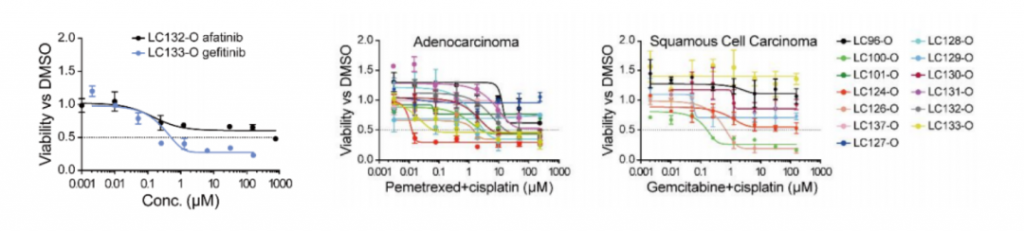
药敏测试及肺癌靶向药物的疗效预测
作者基于LCOs进行了为期一周的药物敏感性测试并对肺癌靶向药物的疗效预测,可获得早于NGS检测的疗效预测结果,并与基因突变结果一致。另外,为期一周的药物敏感性试验还代表了肿瘤对化疗的反应异质性。
结语
作者将InSMAR-chip与类器官技术相结合,成功将药敏试验缩短至一周,通过与PDX模型、基因突变和临床实际疗效的对比,均证实能够预测体内肿瘤对抗癌药物的反应,具备药物筛选的潜力。
清华大学医学院刘鹏副教授、北京大学人民医院胸外科王俊院士、北京航空航天大学陈晓芳副教授为该论文通讯作者,清华大学医学院博士胡亚伟、北京大学人民医院胸外科副主任医师隋锡朝为本文共同第一作者。
科途医学是一家专注于肿瘤类器官技术研发与商业转化的CRO公司,提供临床前药效评价、生物标志物研究、联合用药等研究服务。
类器官相关产品相关类器官产品推荐
| 试剂盒/模型 | 产品 |
|---|---|
| 类器官培养试剂盒 | 乳腺癌肿瘤类器官培养试剂盒 |
| 非小细胞肺癌类器官培养试剂盒 |
|
| 卵巢癌类器官培养试剂盒 | |
| 胃癌肿瘤类器官培养试剂盒 | |
| 结直肠癌肿瘤类器官培养试剂盒 | |
| 宫颈癌肿瘤类器官培养试剂盒 | |
| 类器官模型 | 胃癌类器官模型 |
| 胃印戒细胞癌类器官模型 | |
| 肝癌类器官模型 | |
| 胰腺癌类器官模型 | |
| 膀胱癌类器官模型 | |
| 三阴性乳腺癌类器官模型 | |
| 非小细胞肺癌类器官模型 | |
| 滑膜肉瘤类器官模型 | |
| 肝内胆管癌类器官模型 | |
| 胆管癌类器官模型 |




